아연염소 전지와 아연브롬 전지
페이지 정보
작성자 관리자 댓글 0건 조회 7,067회 작성일 15-01-30 12:45본문
아연은 값싸고 가공하기 쉬운 대포적인 마이너스 극 재료이다. 매우 쉽게 이온화하므로 마이너스 전위를 잘 유지해준다. 한편 염소와 브롬은 모두 할로겐 원소의 일종으로 주기율표에서 7B족에 속하는 원소이다. 가장 바깥쪽 궤도를 돌고 있는 전자가 모두 7개로 나머지 1개만 더 얻으면 주기율표 오른쪽 끝의 아르곤(Ar)이나 크립톤(Kr) 처럼 안정적인 원소가 된다, 따라서 이들 원소는 항상 주변에 있는 것이 무엇이든 달려들어 반응을 일으키려 한다, 늘 하나 더! 라고 왕성하게 외치고 있는 것이 바로 할로겐 원소이다,
아연.염소 전지와 아연브롬 전지는 비슷한 점이 많다, 양쪽 모두 마이너스 극에서 똑 같은 반응이 일어나며 염소나 브롬이 물을 이용하여 유체상태로 아연이 들어있는 반응탱크로 들어간다는 점도 똑같다, 그러나 보통의 전지와 달이 양쪽 극의 활물질이 충전할 때만 서로 가까이하고 그 이외에는 서로 떨어져있다. 앞서 전지의 활물질을 연인사이에 비유했는데 이 경우에는 연인보다는 1주일에 1번 만나는 주말부부에 가까울 것이다. 큰 차이점이라면 염소는 물에 용해되지 않지만 브롬은 물에 용해되기 쉽다. 따라서 아연염소 전지에는 격리판이 없다,
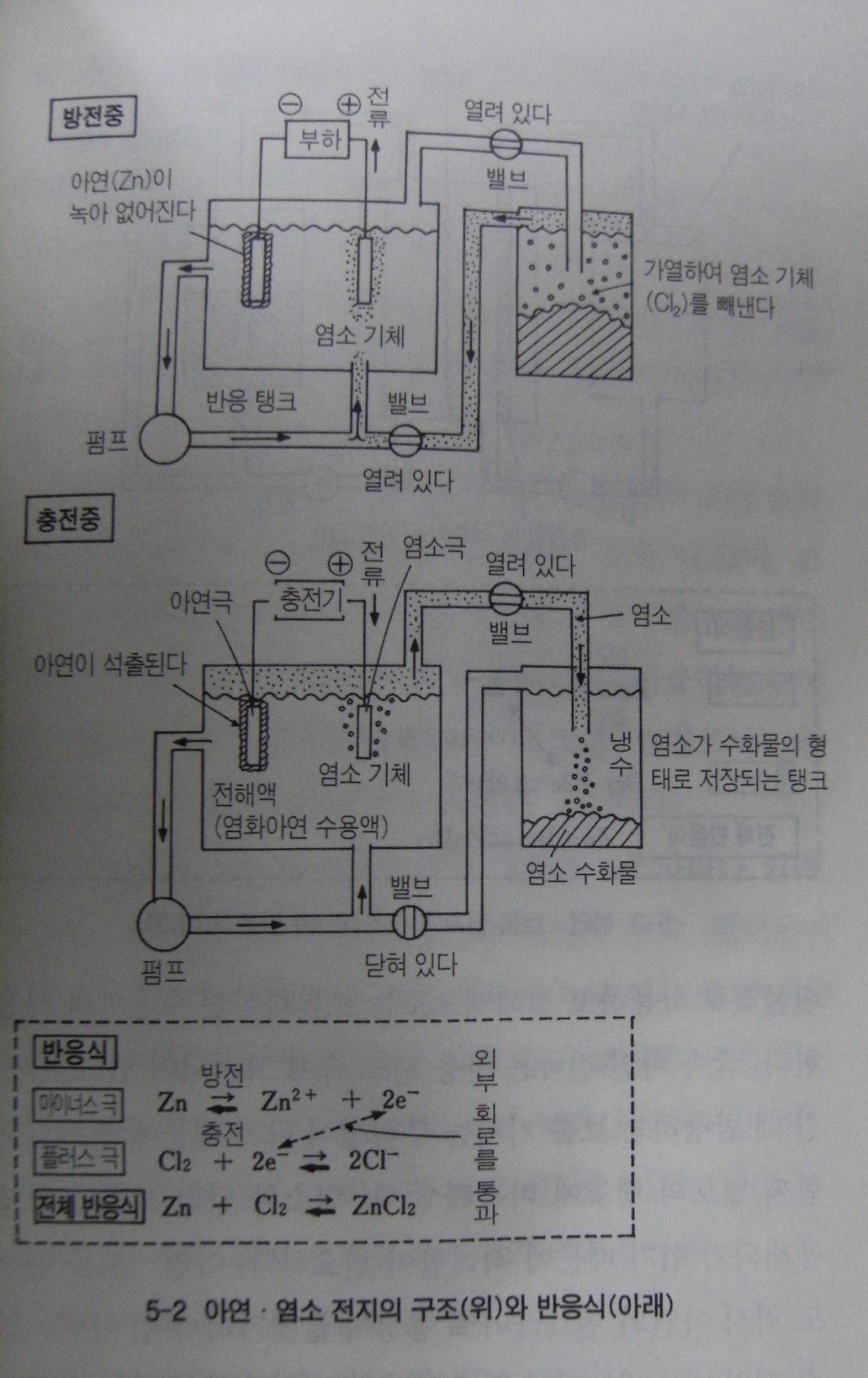
아연염소 전지는 그림과 같이 플러스 극에 염소,마이너스 극에 아연을 활물질로 이용하며 염화아연 수용액을 전해액으로 사용하는 액순환형 전지이다. 금소아연 전극은 반응탱크 속에 고정되어있고 염소는 플러스극의 다공질 흑연 전극 표면에 흡착되어 반응을 일으킨다, 충전하면 마이너스 극에서는 아연이 석출되고 플러스극에서는 염소기체가 발생한다, 발생한 염소기체는 옆에 있는 탱크 속으로 흘러 들어가 6도 이하로 냉각된 물에 녹아 염소수화물 형태로 저장된다, 방전할 때는 이 수화물을 가열하여 염소기체를 발생시켜 플러스 극으로 보낸다, 아연은 아연이온과 전지로 변하고 이 전자는 외부회로를 통해 염소기체로 전달되어 염소를 음이온인 염화이온으로 변화시킨다, 이렇게 하여 각각 이온이 되면서 발전을 계속하는 것이다, 충전할 때는 반대로 이온이 원래의 원소로 되돌아간다.
이 전지는 방전에 따른 생성물이 없고 충전과 방전이 일어날 때의 전압변동이 적다. 그러나 충전할때 아연의 덴드라이트[비늘모양의 결정]가 형성되어 두 전극 사이가 단락 되기 쉬운 것이 큰 문제로 지적되고 있다.
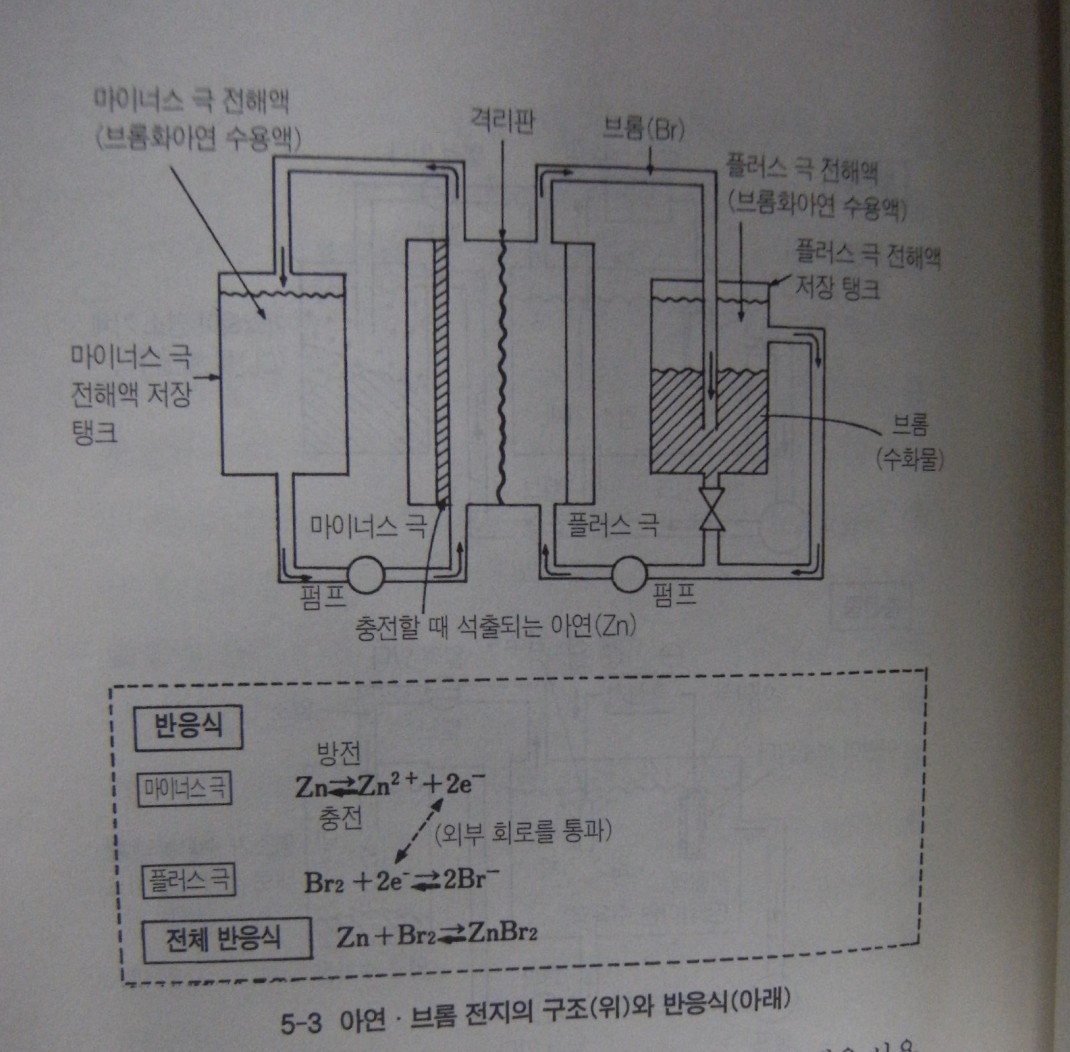
이번에는 아연브롬 전지를 살펴보자. 그림과 같이 플러스극에 브롬 마이너스극에 아연을 활물질로 사용하고 전해액으로는 브롬화아연 수용액을 사용한다. 금속아연전극은 반응 탱크속에 고정되어있고 충전할 때 발생하는 브롬기체는 부식성이 크기 때문에 전해액과 함께 별도의 탱크에 비축해둔다. 염소와 달리 브롬은 물에 용해되기 쉽기 때문에 격리판이 필요하다, 아연브롬 전지도 역시 아연의 덴드라이트 형성이 골치거리이며 아연염소 전지처럼 냉동기가 필요하지 않고 상온에서 작동한다.
댓글목록
등록된 댓글이 없습니다.


